
Charakterystyka cyklodekstryn
Budowa, właściwości i otrzymywanie cyklodekstryn
Cyklodekstryny zwane inaczej cykloamylozami lub cyklooligoamylozami to cykliczne oligomery glukozy. Po raz pierwszy związki te zostały otrzymane w roku 1891 przez Villiersa w reakcji degradacji skrobi. W roku 1904 opisano je jako oligosacharydy a w roku 1938 Freudenberg określił ich budowę. W następnych latach określono ich masę cząsteczkową i zsyntetyzowano pierwsze kompleksy inkluzyjne cyklodekstryn. Obecnie trwają intensywne badania tych związków i znajdują one zastosowanie w wielu dziedzinach nie tylko chemii [1].
Cyklodekstryny otrzymuje się najczęściej ze źródeł naturalnych poprzez enzymatyczną degradację skrobi. W procesie tym uczestniczą enzymy zwane glukotransferazami cyklodekstrynowymi (CGT-azami) oraz inne enzymy z grupy amylaz. Glukotransferazy to enzymy pochodzenia bakteryjnego. Ich działanie polega na katalizie w pierwszej kolejności reakcji rozszczepienia łańcuchów polisacharydowych, a w drugiej kolejności na cyklizacji tychże łańcuchów. W wyniku tego procesu powstaje mieszanina cyklicznych i łańcuchowych maltooligosacharydów. Odpowiednie cyklodekstryny otrzymuje się przez dodanie do mieszaniny czynników selektywnie strącających np. toluenu które kompleksują cyklodekstryny. Dzięki temu otrzymujemy jedynie prawoskrętne enancjomery odpowiednich cyklodekstryn charakteryzujące się bardzo wysoką czystością enancjomeryczną. Enancjomery lewoskrętne są związkami syntetycznymi [2].
Do najczęściej spotykanych cyklodekstryn zaliczamy α-, β- i γ-cyklodekstryny. Są to związki krystaliczne i jednorodne zbudowane odpowiednio z 6, 7 i 8 reszt α-D-glukozy połączonych ze sobą wiązaniem α-1,4-glikozydowym. (rys.)
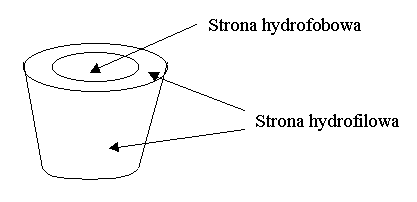
Pierścień zawiera dwa rodzaje grup hydroksylowych: grupy –OH znajdują się w pozycji C-6, oraz grupy hydroksylowe w pozycji C-2 oraz C-3. Grupy –OH(2),(3) rozmieszczone są po jednej stronie pierścienia a grupy –OH (6) leżą po drugiej stronie.
Pierścień α-, β- i γ- cyklodekstryn, ustawienie cząsteczki, stopień wiązania wodorowego pomiędzy grupami hydroksylowymi C-2 i C-3 jest różny dla każdej z tych cyklodekstryn. Grupy hydroksylowe C-2 i C-3 sąsiednich jednostek glukozy w β-cyklodekstrynie są skierowane w taki sposób, że bardzo silnie oddziałują na siebie. W wyniku tego słabo oddziałują z polarnymi cząsteczkami wody. W przypadku pierścienia α-cyklodekstryny, gdzie mimo że naprężenia w pierścieniu są większe niż w β-cyklodekstrynie, grupy hydroksylowe układają się w taki sposób że oddziałują ze sobą znacznie słabiej. Dlatego możliwe jest dużo silniejsze oddziaływanie tych grup z cząsteczkami wody. W rezultacie α-cyklodekstryna jest dużo lepiej rozpuszczalna w wodzie niż β-cyklodekstryna. W cząsteczce γ-cyklodekstryny występuje jeszcze mniejsze oddziaływanie między grupami hydroksylowymi sąsiednich jednostek glukozowych, przez co cyklodekstryna ta najlepiej rozpuszcza się w wodzie. β-cyklodekstryna jest słabo rozpuszczalna w większości rozpuszczalników organicznych, ale za to rozpuszcza się znacznie lepiej, gdy zastosujemy układ rozpuszczalnik organiczny:woda. Generalnie dla większości cyklodekstryn rozpuszczalność zmniejsza się wraz ze wzrostem stężenia niewodnego rozpuszczalnika. Wyjątkiem są tutaj etanol, metanol, acetonitryl, gdzie maksymalna rozpuszczalność cyklodekstryny przypada na 20%, 30% stężenia tego rozpuszczalnika. Najlepszymi rozpuszczalnikami cyklodekstryn są DMF oraz DMSO. Rozpuszczalność kompleksów cyklodekstryn może dość istotnie różnić się od rozpuszczalności czystych cyklodekstryn. Jest to uzależnione przede wszystkim od rodzaju „cząsteczki gościa”. Niektóre związki tworzą nierozpuszczalne kompleksy, a inne tworzą bardzo dobrze rozpuszczające się kompleksy w wielu przypadkach znacznie lepiej niż w przypadku nieskompleksownych cyklodekstryn.
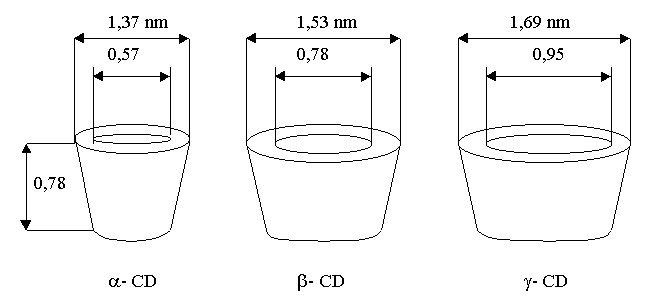
Rysunek przedstawia budowę strukturalną cyklodekstryn [3]. Średnica torusa od strony drugorzędowych grup hydroksylowych jest znacznie większa niż od strony pierwszorzędowych grup hydroksylowych. Obecność tych grup nadaje obu końcom torusa charakter hydrofilowy. Wnętrze pierścienia jest apolarne, hydrofobowe o właściwościach zbliżonych do centrów aktywnych w enzymach. Dzięki takiej budowie może zachodzić selektywne inkludowanie innych cząsteczek lub jonów w kompleksie typu „gospodarz- gość” [4].
Jedną z kolejnych właściwości chemicznych cyklodekstryn jest to, że ulegają reakcji hydrolizy choć są dużo bardziej odporne na hydrolizę kwasową niż skrobia. Silne kwasy takie jak kwas solny, siarkowy hydrolizują cyklodekstryny (przez otwarcie pierścienia) do mieszaniny oligosacharydów. Szybkość hydrolizy wzrasta wraz ze wzrostem stężenia kwasów i wzrostem temperatury. Zasady nie powodują hydrolizy cyklodekstryn nawet jeśli zwiększymy ich stężenie lub będziemy przeprowadzać tą reakcję w podwyższonej temperaturze. Cyklodekstryny ulegają również biodegradacji poprzez hydrolizę α-amylazami i są dużo bardziej odporne na tą reakcję niż skrobia.
Cyklodekstryny mogą również ulegać reakcji utleniania. Grupy hydroksylowe utleniają się do grupy aldehydowej lub kwasowej. β-cyklodekstryna dość łatwo ulega utlenieniu w wyniku reakcji z wodą utlenioną oraz podchlorynem sodu.
Cyklodekstryny nie są związkami toksycznymi, co potwierdziły liczne badania doświadczalne przeprowadzone na wielu gatunkach zwierząt. Grupie szczurów przez okres 3 miesięcy podawano karmę zawierającą niewielką domieszkę β-cyklodekstryny, a po zakończeniu tego okresu przeprowadzono wnikliwe badania i wyniki porównano z badaniami wykonanymi na grupie szczurów których dieta nie zawierała cyklodekstryny. Stwierdzono, że nie zaobserwowano żadnych patologicznych zmian we krwi i narządach wewnętrznych tych zwierząt. Nie stwierdzono również podrażnienia skóry, oczu, górnych dróg oddechowych oraz nie wykryto żadnych niekorzystnych zmian mutagennych. Dlatego cyklodekstryny mogą być stosowane w przemyśle farmaceutycznym. Nie stanowią żadnego zagrożenia dla zdrowia i życia organizmów żywych [1].
Kompleksy inkluzyjne cyklodekstryn
Kompleksy inkluzyjne typu „gospodarz- gość” powstają w wyniku niekowalencyjnych oddziaływań między poszczególnymi cząsteczkami. Procesy inkluzyjne polegają na rozpoznaniu chemicznej oraz przestrzennej budowy cząsteczki gościa przez dużo większą od niej cząsteczkę gospodarza. Jednym z wielu przykładów cząsteczek gospodarza są cyklodekstryny. Kompleksują one we wnętrzu pierścienia wiele jonów oraz związków organicznych. Jednym z warunków tworzenia się takich kompleksów jest to, że cząsteczki gościa muszą w całości albo przynajmniej w znacznej części wniknąć do wnęki cyklodekstryny [5]. Tworzenie kompleksów może zachodzić w roztworze wodnym jak i na nośniku stałym. W ogromnej większości powstających w ten sposób kompleksów stosunek molowy cząsteczki gościa do gospodarza wynosi 1:1, choć znane są również przykłady w których stosunek ten wynosi 2:1, 1:2 lub 2:2 [6].
Schemat tworzenia się kompleksu gospodarz- gość 1:1
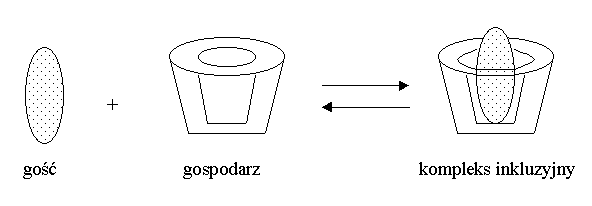
Schemat tworzenia się kompleksu gospodarz- gość 2:1
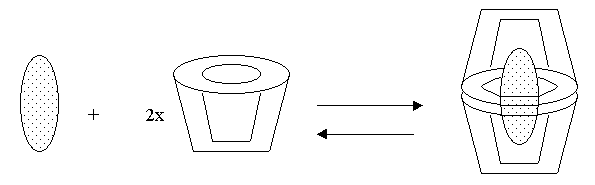
Za powstawanie trwałych kompleksów odpowiedzialne są siły van der Waalsa, wiązania wodorowe, oddziaływania typu dipol – dipol itp. W większości przypadków proces kompleksowania jest regioselektywny i stereospecyficzny, a cyklodekstryny wykazują selektywność substratową.
Czynnikami powodującymi stereoselektywne tworzenie się kompleksów jest kształt i wielkość wnęki cyklodekstryny. Głębokość wnęki wynosi 8 Å. Szerokość zależy od liczby jednostek glukozowych tworzących pierścień. Tylko cząsteczka gościa posiadająca odpowiedni kształt i wielkość może zostać zainkludowana we wnęce cyklodekstryny.
Niepodstawione cyklodekstryny moją sztywną strukturę ze względu na wewnątrzcząsteczkowe wiązania wodorowe pomiędzy grupami wodorotlenowymi –OH(2),(3) sąsiadujących jednostek glukozowych. Modyfikacje grup –OH(2), -OH(3) i –OH (6) w istotny sposób zmieniają właściwości fizyczne wnęki oraz strukturę tworzących się kompleksów inkluzyjnych. Modyfikacja grup –OH(2) i –OH(6) przez przyłączenie grupy metylowej powoduje, że wnęka zwiększa swoją głębokość, dzięki czemu cząsteczki gościa mogą wnikać głębiej i być lepiej inkludowane [2]. Odpowiednie pochodne cyklodekstryn wykazują również właściwości selektywnego i specyficznego kompleksowania cząsteczek gości, co wykorzystuje się do rozdzielania racematów [1].
Zastosowanie cyklodekstryn
Cyklodekstryny znalazły wiele zastosowań laboratoryjnych i przemysłowych. Zdolność tworzenia przez nie kompleksów inkluzyjnych pozwala na ich szerokie zastosowanie w przemyśle spożywczym, farmaceutycznym oraz kosmetycznym. Kompleksy wykorzystuje się jako stabilizatory substancji czułych na działanie światła, temperatury, tlenu. Przykładem może być tutaj witamina A, która jest silnie podatna na działanie światła i czynników utleniających. Dzięki tworzeniu kompleksów z cyklodekstryną jest dużo bardziej odporna na działanie powyższych czynników i proces utleniania zachodzi znacznie wolniej. Podobne kompleksy może tworzyć witamina D3 [1].
Przez chemiczną modyfikację aktywności cząsteczek gościa cyklodekstryny chronią je przed inkludowaniem z innymi cząsteczkami a dzięki blokowaniu niektórych grup funkcyjnych powodują, że cząsteczki gościa reagują selektywnie. Modyfikują również fizykochemiczne właściwości cząsteczek gościa, powodując zwiększenie lub zmniejszenie rozpuszczalności, zmianę barwy, zanik nieprzyjemnego zapachu lub smaku. Stosuje się je również w celu zwiększenia lub zmniejszenia aktywności chemicznej danej molekuły oraz do jej ochrony przed degradacją w procesach fotolizy i hydrolizy. Cyklodekstryny szeroko rozpowszechnione są także w przemyśle spożywczym jako stabilizatory margaryny, masła i majonezu. Dzięki inkluzji cząsteczek między innymi środków ochrony roślin z cyklodekstryną możliwa jest sprzedaż tych związków w postaci łatwego w pakowaniu, przechowywaniu i transporcie proszku. Proszek taki wykorzystywany jest również do zwiększenia trwałości i wydłużenia aktywności wielu środków owadobójczych takich jak np. DDVP [4].
Z uwagi na budowę cyklodekstryn znalazły one zastosowanie do konstrukcji chemicznych modeli enzymów. Zaletą tych modeli jest to, że wykazują one specyficzność substratową, a katalizowane przez nie procesy mają charakter stereospecyficzny. Dzięki temu powstaje tylko jeden z możliwych produktów reakcji i dlatego możliwe jest ich zastosowanie do przyspieszania wielu reakcji oraz kontrolowania ich przebiegu. Grupy hydroksylowe
–OH(2),(3) w cyklodekstrynie spełniają rolę centrum aktywnego podobnego do tego jaki występuje w enzymach. Mechanizm katalizy jest spowodowany stereochemią procesu wnikania cząsteczki substratu i utworzeniu kompleksu „gospodarz-gość. Zasadę działania takiego modelu możemy wyjaśnić na przykładzie hydrolizy octanu fenylu do kwasu octowego katalizowanego przez cyklodekstrynę (rys.). Ze względu na budowę pierścień aromatyczny wnika do wnęki cyklodekstryny a pozostała część cząsteczki reaguje z grupami hydroksylowymi cyklodekstryny. W wyniku przegrupowania i rozpadu wiązań powstają produkty: fenol oraz kwas octowy a także zostaje odtworzona cząsteczka katalizatora. Kataliza jest rezultatem efektu ”mikrorozpuszczalnika” heterogenicznej luki cyklodekstryny [1].

Ponieważ cyklodekstryny są cząsteczkami optycznie czynnymi służą one również do rozdzielania związków chiralnych np. węglowodorów. Dzięki temu że posiadają one selektywne zdolności inkludowania cząsteczek wykorzystuje się je do chromatograficznego jak również i elektroforetycznego rozdzielania enancjomerów. W chromatografii kolumnowej HPLC wykorzystywany jest żel krzemionkowy modyfikowany cyklodekstrynami a w chromatografii gazowej cyklodekstryny stanowią fazy stacjonarne kolumn kapilarnych. Na cyklodekstrynach jako fazach stacjonarnych można rozdzielić izomery strukturalne, geometryczne oraz diastereoizomery. Jest to wykorzystywane przy analitycznym rozdziale izomerów feromonów, leków oraz zanieczyszczeń. [4]
Cyklodekstryny mogą również tworzyć dimery, w których poszczególne jednostki połączone są wiązaniami C-S oraz C-N. Dimery, które otrzymano w wyniku reakcji pierwszorzędowej strony cząsteczki cyklodekstryny z odpowiednimi substratami wykazują duże zdolności wiążące porównywalne z podobnymi właściwościami przeciwciał w organizmach żywych. Ich zdolność do silnego wiązania substratów przypomina działanie enzymów i dlatego służą one jako syntetyczne enzymy w wielu reakcjach przebiegających poprzez wytworzenie kompleksu inkluzyjnego.[1]
Cyklodekstryny mogą być również wykorzystane do modyfikacji elektrod (przede wszystkim elektrody złotej) przez utworzenie monowarstwy cyklodekstryny na powierzchni tej elektrody w wyniku samoorganizacji z roztworu. Najprostszym sposobem modyfikowania elektrod jest adsorpcja fizyczna. Cyklodekstryna adsorbuje się na kapiącej elektrodzie rtęciowej tworząc zwartą warstwę. Pochodne cyklodekstryn z grupami zawierającymi siarkę tworzą na powierzchni złota wysoko uporządkowane monowarstwy. Te monowarstwy umożliwiają śledzenie relacji pomiędzy strukturą molekularną a właściwościami cyklodekstryn.
komentarze
Copyright © 2008-2010 EPrace oraz autorzy prac.